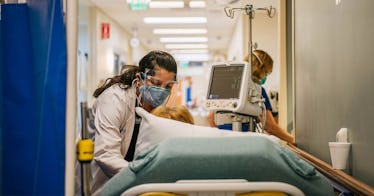
美国默克制药公司刚刚向FDA申请了molnupiravir的紧急使用授权,这是一种与Ridgeback Biotherapeutics合作开发的片剂,用于治疗轻至中度的埃博拉病例新型冠状病毒肺炎.如果获得批准,这种药物将是第一种口服抗病毒药物,并可能改变目前对抗这种疾病的游戏规则。
目前,COVID患者在入院时通常会服用抗病毒药物瑞德西韦和通用类固醇地塞米松。根据FDA的紧急使用授权,单克隆抗体疗法也被用作COVID治疗。
Molnupiravir不同,因为它是由埃默里大学的科学家开发的,专门用于治疗新型冠状病毒肺炎.它是一种有效的核糖核苷类似物,可以抑制导致COVID-19的冠状病毒的复制,而且它已被证明对病毒的“最常见”变体有效,这一描述符似乎包括了高度传染性的病毒三角洲变体.
默克公司正在向FDA申请紧急使用授权,这与所有COVID-19疫苗最初获得的授权是相同的Pfizer-BioNTech疫苗继续分发下。该公司关于该药物有效性和安全性的证据来自临床试验,该试验表明,对已感染但未发展为严重COVID-19的人使用molnupiravir非常有效。该药物用于非住院患者,至少有一个风险因素这使他们的病情有可能恶化到需要住院治疗的地步。
在研究进行到一半时,服用molnupiravir的患者比服用安慰剂的患者表现明显更好默克公司.他们面临住院或死亡的可能性降低了一半(7.3%对14.1%),在29天内没有人死亡,而服用安慰剂的8人确实去世了。
美国政府已经签署了一份供应170万个疗程molnupiravir的合同,每个疗程的价格为700美元,该公司还与世界其他国家政府签订了供应和预先购买协议,以分配其计划在今年年底前生产的1000万个疗程中的剩余部分。此外,默克公司还将该药授权给了几家仿制药制造商,这些制造商预计将生产molnupiravir,并在100多个中低收入国家销售。
申请的molnupiravir紧急使用授权仅适用于成人,因此感染COVID-19的儿童将没有资格获得它,至少目前还没有。目前还不清楚是否疫苗生产厂家在美国,默克公司将寻求FDA对18岁以下患者的任何类型的授权。
因此,虽然它对有小孩的父母的直接使用可能有限,但对COVID-19患者有效药物的存在,以及现在广泛可用的疫苗,对我们这些渴望迎来大流行后世界的人来说是个好消息,在这个世界中,COVID-19存在,但不会像过去近两年那样彻底破坏世界。